研究内容PROJECT
トップページ > お問い合わせ
プロジェクト概要
合成(同化)と分解(異化)との動的平衡の維持は,生命活動において極めて重要です。また,このバランス制御の破綻により様々な疾患が引き起こされます。例えば、多くの神経・筋変性疾患は細胞質にタンパク質の凝集体・封入体を伴う「タンパク質たまり病」です。また近年,難治性多発性骨髄腫の治療薬として開発されたプロテアソーム阻害薬に代表されるように,がん細胞内のタンパク質分解系を止めることで,タンパク質蓄積によるストレス負荷から細胞死を誘導する治療法も採られています。このように分解系を制御する「手法」は、分野横断的に治療に直結することが予想されます
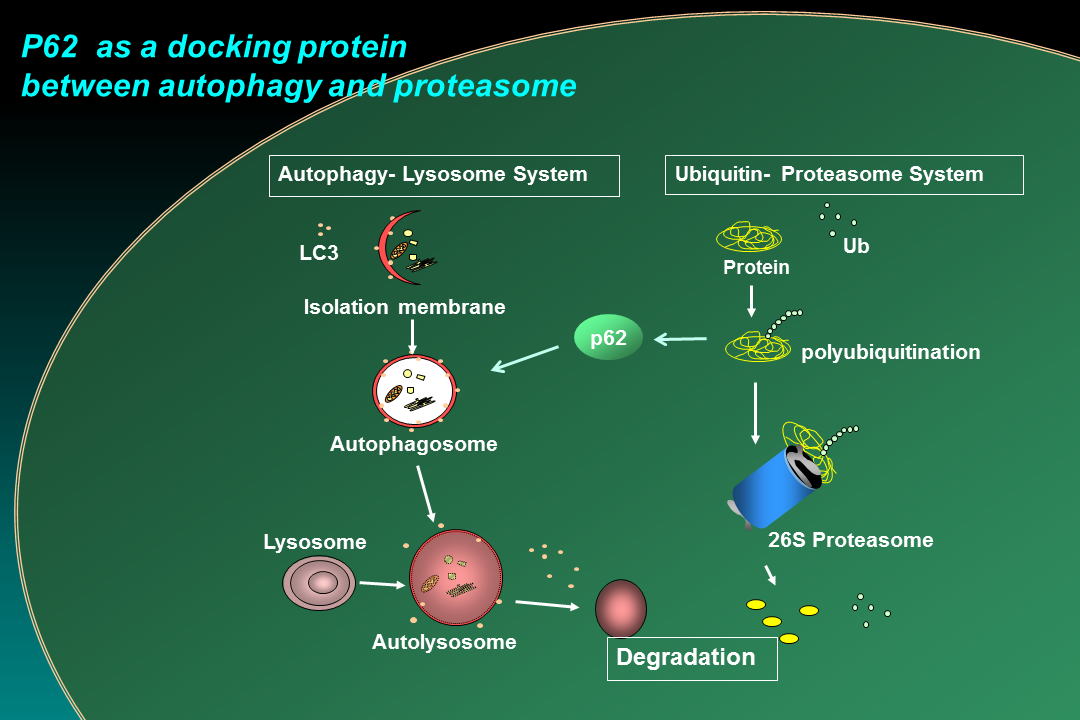
ユビキチン・プロテアソーム系は,ユビキチン化されたタンパク質がプロテアソームで「選択的」に分解するプロセスです。これに対して,オートファジーは,細胞質内のタンパク質や小器官を自食胞(オートファゴソーム)と呼ばれる二重脂質膜で包み込み,これをリソソームに輸送して分解することから,非選択的(バルク)な分解機構と捉えられてきました。しかし,近年,p62(sequestosome
1)をはじめとするドッキングタンパク質により,ユビキチン化タンパク質がp62との結合を介して選択的にオートファゴゾーム内に取り込まれて分解されるメカニズムが明らかとなり,細胞内の二大分解機構の相互連鎖が注目されています。さらに,オートファジーは,ミトコンドリア,小胞体,リソソームの細胞内クリアランスにも関与し,これら小器官の「品質管理」としても重要な機能を担っていることも明らかになりました。このように,「分解機構」の重要性は,人体を構成する全臓器に,そして,全ての疾患領域に及んでいるといっても過言ではありません。
本プロジェクトは,ハイスループット・アフィニティー精製をコア技術として,骨髄腫,リウマチ,筋変性疾患,がんの各分野で,「分解系」に関する先進的研究を行っているチームが結集して,分子病態の解明と新規治療法開発に向けて分野横断的かつ集約的に取り組んでまいります。
統一目標は「分解機構の解明と人為的制御法(manipulation)の開発」です。
しかし,これらの研究成果は,全臓器に及ぶ「分解系」の普遍性からも明らかなように,今後さまざまな疾患領域との関連性を生み,研究分野の裾野は益々広がっていくことが予想されます。さらに多くの研究者の方々への本プロジェクトの参加を期待しております。
プロジェクトリーダー
医学科 生化学分野 主任教授
宮澤 啓介
【本研究プロジェクトのキーワード】
ユビキチン,プロテアソーム,オートファジー,リソソーム,小胞体ストレス,アグリソーム
アフィニティ―ビーズ技術
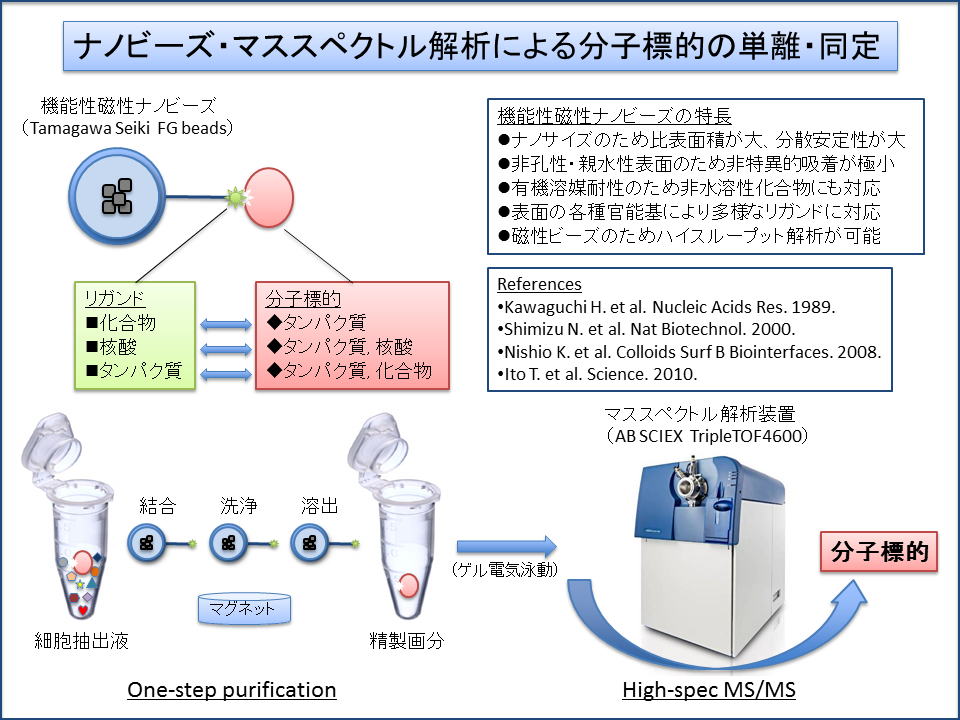
本学の半田 宏 教授らが開発した機能性磁性ナノビーズ(FGビーズ)は,優れた特長を有しているため、種々のリガンド(化合物, 核酸, タンパク質など)を容易に固相化でき、リガンドに結合する分子標的を迅速に単離することが可能です。
リガンドを固相化したFGビーズと細胞抽出液とを混ぜて結合させた後、洗浄液および溶出液の中で、磁気を用いた分離・分散行程を連続して行うことにより、ワンステップで精製画分が得られます。その後、必要に応じてゲル電気泳動により分離を行い、マススペクトル解析により同定します。
バナースペース
東京医科大学 分子標的探索センター
[事務室]
〒160-8402
東京都新宿区新宿6-1-1
第一校舎 一階 生化学研究室内
TEL 03-3351-6141 (内線:244)
FAX 03-3351-6466